LA PIRFENIDONA MEJORA LA ENFERMEDAD POR HÍGADO GRASO
- Escrito por Dr.Poo
- Publicado en Fibrosis Hepática
La enfermedad por hígado graso no alcohólico (EHGNA) es una verdadera pandemia a nivel mundial. Se estima que en la actualidad es la primera causa de enfermedad crónica en el mundo, más frecuente incluso que el daño por alcohol, virus o auto-inmunidad. Una de las formas más avanzadas de la EHGNA es aquella que provoca ruptura celular e inflamación, conocida como esteatohepatitis (en inglés abreviada como NASH). Solo en los EEUU, en el año 2015, se estimó que la población afectada por esta enfermedad era de 83 millones de personas con un incremento del 21% para el 2030, lo cual da una cifra estimada de 100.9 millones de casos. Se calculó que el impacto económico para el 2030 será de $1,000 trillones de dólares en los EEUU y de alrededor de $334 billones de euros en Europa. Por ello, diversos investigadores han propuesto simular la enfermedad en modelos experimentales, con el fin de conocer los mecanismos moleculares del daño e identificar nuevos agentes terapéuticos.
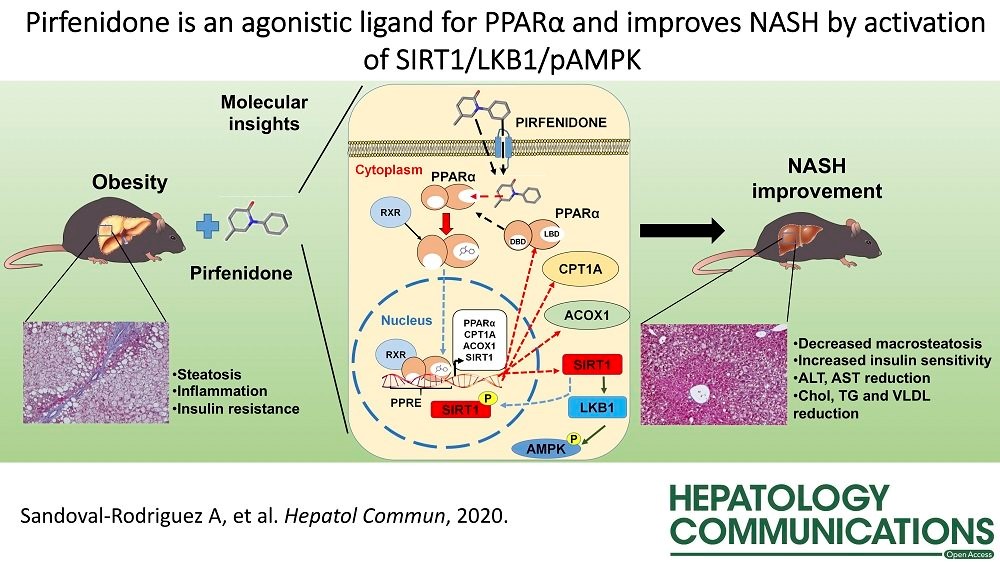
El Dr. Juan Armendariz Borunda y un grupo de investigadores del Instituto de Biología Molecular y Terapia Génica, de la Universidad de Guadalajara y del Instituto Tecnológico de Monterrey, campus Zapopan, en Jalisco, en colaboración con investigadores del Instituto Pasteur de Lille Francia, acaban de publicar en la prestigiosa revista Hepatology Communications (marzo de 2020) un interesante trabajo que tenía como objetivo evaluar los efectos de la Pirfenidona de Liberación Prolongada (PFD-LP) en las alteraciones inducidad por la esteato-hepatitis (NASH). Entérate de cómo este grupo de investigadores mexicanos lograron demostrar que la pirfenidona, es benéfica en un modelo experimental de enfermedad por hígado graso en roedores.
Metodología: Se realizaron diversos experimentos; unos de ellos conocidos como in vitro (con células hepáticas en cultivo) y otros en vivo, con ratones macho de 4 semanas de vida, de 20-25 g de peso inicial, en apego a las normas nacionales e internacionales de cuidado de animales y con la aprobación del Comité de Ética e Investigación de la Universidad de Guadalajara.
 Después de un período de 1 semana de aclimatización a las condiciones del laboratorio, los ratones fueron divididos en cinco diferentes grupos:
Después de un período de 1 semana de aclimatización a las condiciones del laboratorio, los ratones fueron divididos en cinco diferentes grupos:
Grupo 1: Dieta estandarizada y agua libre durante 8 semanas
Grupo 2: Dieta alta en grasa (DAG) y bebida alta en carbohidratos (BAC) por 8 semanas, lo cual induce los cambios bioquímicos e histológicos de NASH
Al terminar la semana 8, los ratones fueron divididos, al azar, en dos grupos
Grupo 3. DAG y BAC, por 8 semanas adicionales (hasta la semana 16), para simular seguir con NASH, sin tratamiento
Grupo 4. DAG y BAC por 8 semanas adicionales (hasta la semana 16), tratados con PFD-LP (dosis de 300 mg/kg) todos los días, disuelto en su alimento.
Al terminar la semana 8, se incluyó un grupo control adicional que simula el tratamiento usual del padecimiento
Grupo 5: Dieta de cambio, en la cual los ratones con cambios de NASH de 8 semanas suspenden la DAG y BAC e inician con dieta estandarizada y agua libre durante 8 semanas más.
Estudios realizados: se realizaron una gran cantidad de evaluaciones, las cuales resumimos en las siguientes categorías.
- Pruebas de función hepática, glucosa y perfil de lípidos
- Curva de tolerancia a la glucosa
- Hormonas metabólicas (insulina, glucagon, leptina y resistina)
- Biopsia hepática
- Medición de citocinas proinflamatorias
- Medición de genes de SIRT-1 (un regulador del metabolismo de la grasa intra-hepática)
- Medición del gen de PPAR alfa (un regulador nuclear de genes involucrados en la regulación de la beta-oxidación mitocondrial y peroxisomal, así como de la captura, unión y transporte de los ácidos grasos).
- Estudios farmacológicos de unión de la PFD-LP al receptores de la molécula llamada PPAR alfa
Resultados: los resultados más relevantes detectados en el grupo tratado con PFD-LP se mencionan a continuación:
- Menor incremento de peso, sin afectar la ingesta calórica diaria.
- Reducción de los niveles de transaminasas (marcadores usuales de inflamación).
- Valores inferiores de colesterol total, C-VLDL y triglicéridos (estas grasas son las que usualmente se elevan en el tejido hepático).
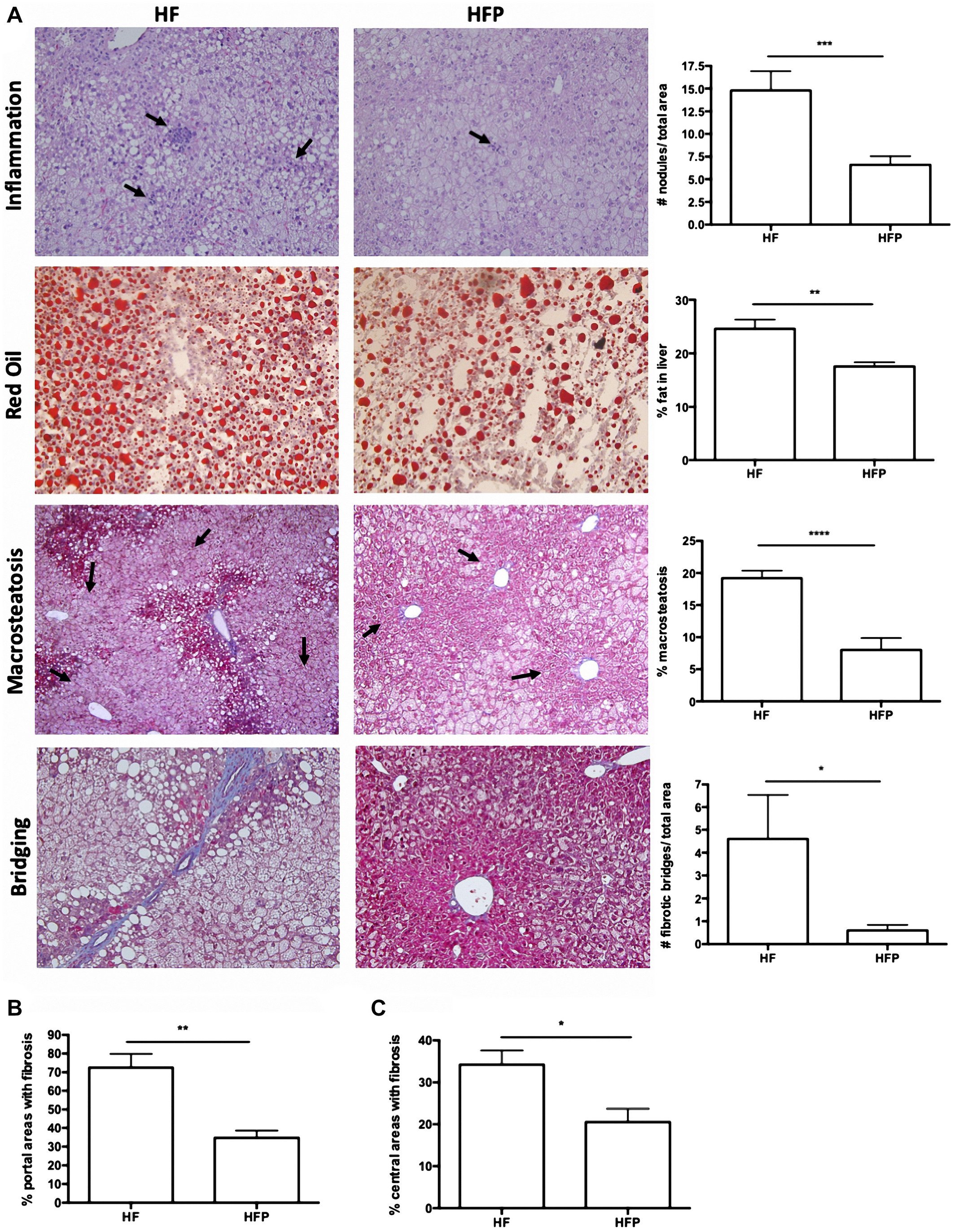
- Menor grado de daño al hígado, menos macro-esteatosis, inflamación, degeneración balonoide del citoplasma de las células, menor fibrosis y menor cantidad de grasa en el cuerpo.
- Mejoría de los niveles de insulina, gluocagon, adiponectina y resistina (mediadores hormonales de daño metabólico).
- Reducción de los niveles de IL-6 y TNF (mediadores moleculares de daño a los tejidos)
- Curva de Tolerancia a la Glucosa con menor resistencia a la acción de la insulina.
- Corrección de la adiposidad de los tejidos observada en los ratones sin tratamiento
- Inducción de SIRT-1, lo cual indica una reducción de la lipotoxicidad y un cambio a la lipolisis lo cual repercute en menor grasa en los tejidos.
- Inducción de la señales inducidas por PPAR alfa, permitiendo una corrección del desbalance observado en los ratones sin tratamiento.
Se demostró además, por técnicas farmacológicas en cultivos celulares, que la PFD-LP es un fármaco agonista directo de los receptores PPAR alfa.
Comentarios: Los autores resaltan que sus resultados demuestran que la PFD-LP induce una mejoría de la mayor parte de los desbalances bioquímicos, metabólicos, genéticos e histológicos observados en ratones sin tratamiento. Tambien enfatizan que la resistencia a la insulina, una condición frecuentemente vista en pacientes con NASH se corrige o disminuye con el tratamiento. Finalmente, los autores concluyen que la demostración de que PFD-LP es capaz de estimular SIRT-1 y PPAR alfa (como ligando específico), se considera un hallazgo de gran relevancia ya que esas dos moléculas son fundamentales para corregir el desbalance en el metabolismo de lípidos en nuestros tejidos.
El Dr. Jorge Luis Poo, Hepatólogo Clínico e investigador del Grupo Mexicano para el Estudio de las Enfermedades Hepáticas, nos menciona que la enfermedad conocida como Esteato-Hepatitis (NASH) es la fase activa de la Enfermedad por Hígado Graso, que tiene el triste potencial de evolucionar a la fibrosis leve y luego a la fibrosis avanzada (F3 y F4 o cirrosis) e incluso hasta el cáncer. De hecho, un tercio de los pacientes con NASH ya tienen fibrosis hepática, es decir cicatrización excesiva dentro del tejido hepático. Lamentablemente esa cicatrización excesiva puede progresar a veces lentamente y a veces rápidamente. Por ejemplo, si existen co-factores en un mismo paciente. Por ejemplo, la co-existencia de obesidad, más diabetes mellitus, más colesterol y trigliceridos elevados, más ingesta de alcohol, puede acelerar el daño. En particular, se considera que la fibrosis avanzada (F3-F4) tiene un mal pronóstico de vida. Es decir, cuando la fibrosis avanzada no se trata, entonces progresa a las complicaciones de la cirrosis (ascitis, hemorragia variceal y encefalopatía, infecciones graves, al cáncer) y a la muerte. Por ello, todos los pacientes con enfermedad crónica deben ser evaluados sobre su grado de fibrosis y proponérseles un tratamiento.
Interesantemente, la PFD-LP ya se comercializa en México como Kitoscell LP. Además de estar disponible en las farmacias nacionales para el tratamiento de la Fibrosis Pulmonar Idiopática existe una amplia experiencia clínica sobre su uso terapéutico en fibrosis hepática. En caso de requerir máyor información sobre este medicamento, te recomendamos ponerte en contacto con tu médico tratante quien es el que mejor conoce tu condición clínica y la necesidad de iniciar o continuar con un tratamiento antifibrótico.
Referencias:
1. Ana Sandoval-Rodriguez, Hugo Christian Monroy-Ramirez, Alejandra Meza-Rios, Jesus Garcia-Bañuelos, Jose Vera-Cruz, Jorge Gutiérrez-Cuevas, Jorge Silva-Gomez,Bart Staels,Jose Dominguez-Rosales, Marina Galicia-Moreno, Monica Vazquez-Del Mercado,Jose Navarro-Partida,Arturo Santos-Garcia,and Juan Armendariz-Borunda. Pirfenidone Is an Agonistic Ligand for PPARα and Improves NASH by Activation of SIRT1/LKB1/pAMPK. Hepatology Communications, 2020;4(3):434-449.
2. Younossi ZM, Koenig AB, Abdelatif D, Fazel Y, Henry L, Wymer M. Global epidemiology of nonalcoholic fatty liver disease—meta-analytic assessment of prevalence, incidence, and outcomes. Hepatology 2016;64:73-84.
3. James M. Paik, Linda Henry, Leyla De Avila, Elena Younossi, Andrei Racila, Zobair M. Younossi. Mortality Related to Nonalcoholic Fatty Liver Disease Is Increasing in the United States. Hepatol Comm November 2019:Volume3,Issue11;Pages 1459-1471


